一、物质结构、元素周期表
元素周期表中共有 118种元素。将元素按照相对原子质量由大到小依次排列,并将化学性质相似的元素放在一个纵列。每一种元素都有一个编号,大小恰好等于该元素原子的核内质子数目,这个编号称为原子序数。在周期表中,元素是以元素的原子序列排列,最小的排行最先。表中一横行称为一个周期,一列称为一个族。
原子的核外电子排布和性质有明显的规律性,科学家们是按原子序数递增排列,将电子层数相同的元素放在同一行,将最外层电子数相同的元素放在同一列。
二、试题解析
1、元素性质呈现周期性变化的根本原因是()
A.元素的相对原子质量递增,量变引起质变
B.元素原子的核外电子排布呈周期性变化
C.元素的原子半径呈周期性变化
D.元素的化合价呈周期性变化
解答: C。
原子半径呈周期性变化,决定了得失电子的能力,也就决定了元素的性质。
2、下列有关说法正确的是()
A.原子的最外层有两个电子的元素都在第Ⅱ A族
B.第Ⅰ A族元素都是典型的金属元素
C.氟、氯、氧、氮四种元素都是第Ⅶ A族的元素
D.第三周期的元素的原子核外都有三个电子层
解答: D。
元素周期表的特殊排列,第三周期元素的原子核外只有三个电子层,钠、镁、铝、硅、磷、硫、氯等。
3、下列关于物质性质变化的比较,不正确的是()
A.原子半径大小: Na> S> O
B.气态氢化物稳定性: HBr< HCl< HF
C.碱性强弱: KOH> NaOH> LiOH
D.还原性强弱: F- > Cl- > Br- > I-
解答: D。
氧化性强的还原性反而弱,所以 D错误。
4、某元素原子 L层电子数比 K层的多 5个,该元素的最高正化合价为()
A.+ 5
B.+ 6
C.+ 7
D.无最高正化合价
解答: D。
5、已知 A、 B、 C、 D均为短周期元素,它们的原子序数依次递增。 A是最外层为一个电子的非金属元素, C原子的最外层电子数是次外层的 3倍; C和 D可形成两种固态化合物,其中一种为淡黄色固体; B和 C可形成多种气态化合物。 A、 B、 C三种元素可以形成离子晶体,该晶体中各元素原子的物质的量之比为 A: B: C= 4:2:3。
请回答下列问题:
( 1)写出 B的原子结构示意图,写出 C和 D形成的淡黄色固体化合物的电子式。
( 2)元素原子的物质的量之比为 A: B: C= 4:2:3的晶体名称为()。
( 3)写出与 A 2 C和 BA 3分子中电子数相同,且仍由 A、 B、 C元素中任意两种元素组成的微粒的符号(举两例)。
( 4)写出由 B、 C元素组成且元素原子质量比为 B: C= 7:12的化合物的化学式。
解答:
( 1) B的原子结构示意图为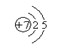
C和 D形成的淡黄色固体化合物——过氧化钠,电子式为: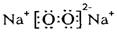
( 2)晶体名称为硝酸铵
( 3)可以举出如 OH-、 NH 4+等。
( 4)由 B、 C元素组成,元素原子质量比为 7:12的化合物可以想到为三氧化二氮,即: N 2 O 3









![]()