1.【思路解析】碳酸钠和碳酸氢钠中阴离子都是碳酸根,所以对应的酸都是碳酸;
碳酸钠水溶液显碱性, pH﹥ 7;胃酸主要是盐酸, NaHCO 3+ HCl= NaCl+ H 2 O+ CO 2↑ ;根据化学反应前后原子数目不变,可以算出化学式;干粉灭火器利用碳酸氢钠来灭火,其灭火原理是产生了二氧化碳,隔绝氧气灭火。
【答案】( 1) H 2 CO 3( 2)>( 3) NaHCO 3+ HCl= NaCl+ H 2 O+ CO 2↑( 4) CO 2
( 5)碳酸氢钠受热分解得到二氧化碳气体,因而隔离了空气而灭火。
【点评】该题考查碳酸盐的相关知识。试题难度中等。
2.能在 pH为 1的溶液中大量共存,且溶液为无色透明的一组物质是()
A. FeCl 3、 CuSO 4、 NaCl
B. BaCl 2、 Na 2 SO 4、 NaOH
C. CaCl 2、 Na 2 CO 3、 AgNO 3
D. K 2 SO 4、 NaNO 3、 NH 4 Cl
【思路解析】溶液为无色透明可以确定不能有带颜色的物质, A中 FeCl 3是黄色的, CuSO 4是蓝色的; B中 BaCl 2和 Na 2 SO 4可以反应生成白色沉淀,不能共存, NaOH也
不能和 PH= 1的酸性物质共存; C中 CaCl 2和 Na 2 CO 3可以反应生成白色沉淀,不能共存, CaCl 2和 AgNO 3可以反应生成白色沉淀,不能共存。
【答案】 D
【点评】该题考查各物质的颜色及相互反应。难度中等。
3.氯气( Cl 2)是有刺激性气味的有毒气体。氯气可与水反应: Cl 2+ H 2 O= HCl+ HClO
(次氯酸)。下图是探究物质漂白性(使有色物质褪色)的实验。
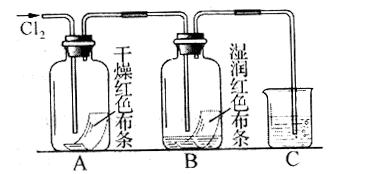
( 1)闻氯气时,在操作上应注意什么问题?
( 2)写出右图 C中 Cl 2与 NaOH溶液反应的化学方程式。(提示: HClO+ NaOH= NaClO+ H 2 O)
( 3)图中实验的现象为 D中布条褪色而 A中布条不褪色,由此可推测具有漂白性
的物质可能有哪些若要证明只有次氯酸有漂白性,还需补做相关的实验,消简要写出实验的步骤和现象。
【思路解析】该题属于实验探究题。( 1)闻气体气味时,应采用扇气入鼻法,防止因
吸入过多气体而中毒( 2) Cl 2与 NaOH溶液反应的化学方程式,可以先参考 Cl 2+ H 2 O= HCl+ HClO和 HClO+ NaOH= NaClO+ H 2 O,综合到一起即可写出,( 3) D比 A中多的是盐酸和次氯酸,所以具有漂白性的物质也可能是这两种物质;若要证明只有次氯酸有漂白性
,应排除盐酸的作用即可,所以可采用取一红色布条,在上面滴加盐酸,布条不褪色。
【答案】( 1)不要把鼻孔凑到容器口去闻氧气的气味。
(或用手在容器口轻轻扇动,让极少量气体飘进鼻孔。)
( 2) Cl 2+ 2 NaOH= NaCl+ NaClO+ H 2 O. ( 3)具有漂白性的物质可能有盐酸和次氯酸。
取一红色布条,在上面滴加盐酸,布条不褪色。
【点评】本题属于典型的实验探究和信息题。第二问化学方程式的书写是难点。试题难度
较大。